To miał być artykuł wyjaśniający medyczne aspekty diagnostyki molekularnej w odniesieniu do chorób nowotworowych, ale historie pacjentów i wypowiedzi lekarzy zwróciły moją uwagę na zupełnie inne – społeczne tory.
Uznałam, że w aktualnej sytuacji – zamiast informacji o osiągnięciach tej nowej gałęzi medycyny – należy ocenić stan diagnostyki molekularnej w polskiej onkologii. Przedstawić oczekiwania i postulaty pacjentów oraz lekarzy w tym zakresie.
Badanie genetyczne skierowało mnie na zupełnie nowe drogi nadziei
czyli o znaczeniu diagnostyki molekularnej w terapii nowotworów
Mój rak to bardzo rzadka choroba, która dotyczy niecałych 0,3% wszystkich zachorowań na nowotwory na świecie. Jak widać, nawet w tak trudnym przypadku badanie genetyczne skierowało mnie na zupełnie nowe drogi nadziei, przedstawiając mi trzy dostępne farmaceutyki oraz dwa badania kliniczne, które być może mogą mi pomóc [1] – pisze 37 letni Rafał Zawidzki chory na Adenoid Cystic Carcinoama (ACC) gruczołowo-torbielowatego raka, bardzo złośliwego, dającego przerzuty do wielu organów. Rafał skorzystał z pomocy działającego od niedawna w Polsce profesjonalnego i niestety drogiego serwisu terapii spersonalizowanej prowadzonego przez niemiecko-węgierską firmę [2]. Po przeprowadzeniu badań genetycznych, przedstawia ona pacjentowi informacje o możliwości aktualnego leczenia na całym świecie, nie tylko zarejestrowanymi już lekami celowanymi, ale i tymi będącymi w badaniach klinicznych.
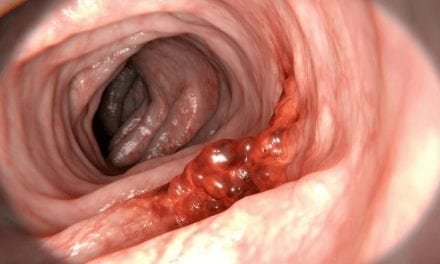
Historia Rafała uświadamia nam, jak bardzo potrzebna jest diagnostyka molekularna w leczeniu chorych onkologicznie. Trafna diagnoza jest podstawą właściwego leczenia i powrotu do zdrowia – to największy medyczny banał, a zarazem bardzo często największe medyczne wyzwanie. W przypadku nowotworów jest ona coraz bardziej zależna – poza wiedzą, doświadczeniem i intuicją lekarza – od wykonania badań molekularnych. Obecnie, aby właściwie zdiagnozować pacjenta onkologicznego w wielu przypadkach trzeba zajrzeć w głąb komórek, aby określić mutacje genów. Do tego onkologowi niezbędne jest badanie patomorfologiczne komórek raka.
Definicja i statystyki nowotworów / raka
W definiowaniu nowotworu na przestrzeni ostatnich 30. lat widać przede wszystkim różnice w określeniu przyczyn tej choroby. Jeszcze trzy dekady temu były one nieznane, a leczenie nowotworów objawowe [3]. Leczono objawy raka, ale nie znano patogenezy różnych rodzajów raka. Współcześnie wiemy, że przyczyną nowotworów jest powstawanie nieprawidłowych genów, czyli zmian genetycznych. Naprawiając je lub niszcząc jesteśmy w stanie zatrzymać proces nowotworzenia.
Postęp, jaki dokonał się w medycynie w okresie ostatniej dekady, zwłaszcza w genetyce, wskazuje, że wraz z rozwojem badań dla ludzkim genomem i oznaczaniem coraz to nowych mutacji genów, będziemy wyróżniali na tej podstawie kolejne rodzaje nowotworów. Być może zamiast posługiwać się terminologią związaną z umiejscowieniem choroby nowotworowej: rak piersi, rak płuca, rak nerki, itd. będziemy mówili o nowotworze związanym z mutacją BRCA, która jest odpowiedzialna zarówno za raka piersi jak i jajnika.
Obecnie blisko 20% pacjentów onkologicznych choruje na nowotwory rzadkie, czyli takie, które dotyczą jednej na dwa tysiące osób. Już w tej chwili możemy opisać około 100 rodzajów samego raka nerki, a przed 10 laty mówiliśmy tylko o dwóch: jasno- i ciemnokomórkowym. Wkrótce więc, będziemy mieli do czynienia głównie z nowotworami rzadkimi. Potrafimy już tworzyć skuteczne, precyzyjnie działające terapie spersonalizowane leczące chorych na określone rodzaje raka. Problem jest w tym, że zarówno diagnoza molekularna nowotworu, jak i nowoczesna terapia jest bardzo złożona, a co za tym idzie droga. Za tą nową sytuacją medyczną nie nadąża nasz system opieki zdrowotnej.
Należy wszelkimi sposobami wzmocnić możliwości polskiej patomorfologii
czyli o dostępności do diagnostyki molekularnej w Polsce
Problemy związane z dostępnością do diagnostyki molekularnej chorych na nowotwory w Polsce dotyczą zarówno zbyt małej liczby patomorfologów, jak i właściwego sytemu prowadzenia i finansowania tych badań, w tym ich refundacji przez NFZ.
Liczba patomorfologów w Polsce jest zbyt mała wobec potrzeb – współczesna diagnostyka patomorfologiczna jest bardzo złożona, ponieważ obejmuje ocenę morfologiczną oraz molekularną. Patomorfolodzy powinni być współuczestnikiem badań genetycznych i molekularnych, a raporty powinny obejmować wszystkie czynniki niezbędne dla rozpoczęcia prawidłowego leczenia. Należy wszelkimi sposobami wzmocnić możliwości polskiej patomorfologii. Konieczne jest również stworzenie prawidłowego systemu prowadzenia badań molekularnych chorych na nowotwory (…) oraz właściwego finansowania [4] – uważa prof. dr hab. n. med. Maciej Krzakowski, Krajowy Konsultant w dziedzinie Onkologii Klinicznej. Obecnie w Polsce praktykuje 360 patomorfologów, a powinno ich być około 500. Pracują oni często w kilku placówkach, są przemęczeni i źle wynagradzani. Problem jest też niewielka liczba studentów wybierających tę specjalizację, aktualnie w trakcie specjalizacji jest 70 osób. Średni wiek patomorfologa w Polsce to aż 60 lat. Z kolei brak możliwości zatrudnienia patomorfologa, ma wpływ na dotrzymanie standardów stawianych ośrodkom onkologicznym.
Jak wygląda w tych warunkach braku: patomorfologów, refundacji oraz systemowego i prawnego zabezpieczenia polska rzeczywistość diagnostyki molekularnej, opisuje na przykładzie badań genetycznych w odniesieniu do niedrobnokomórkowego raka płuca prof. dr hab. n. med. Paweł Krawczyk z Lubelskiego Uniwersytetu Medycznego – Niestety NFZ nie refunduje badań genetycznych, podobnie jak badań patomorfologicznych. W związku z tym badania te mogą być finansowane w ramach umów zawieranych między szpitalami, które chcą leczyć chorych terapiami ukierunkowanymi molekularnie (w ramach tzw. programów lekowych), a laboratoriami genetycznymi. W praktyce jednak badania genetyczne są finansowane przez koncerny farmaceutyczne wprowadzające swoje preparaty do terapii raka płuca. Mimo tej niekorzystnej sytuacji prawnej większość chorych wymagających diagnostyki genetycznej ma dostęp do tego rodzaju badań. Najczęściej procedura przeprowadzenia badania genetycznego odbywa się na zlecenie lekarza onkologa lub pulmonologa, który widzi możliwość zastosowania leczenia ukierunkowanego molekularnie (…) Po przekazaniu materiału do badania genetycznego przez lekarza leczącego chorego lub patomorfologa, zostają przeprowadzone testy molekularne, których wykonanie nie powinno zająć więcej czasu niż 5-10 dni. W pewnych sytuacjach (np. przy wykorzystaniu technik telepatomorfologicznych) czas ten może być skrócony do 3 dni roboczych [5].
Jak na polskie możliwości, jest to sytuacja idealna, ba nawet powiedziałabym na światowym poziomie (przy wykorzystaniu technik telepatomorfologicznych), ale ile laboratoriów w Polsce tak pracuje?
Problem zbyt małej dostępności do badań genetycznych zauważają nie tylko lekarze, ale nawet politycy. W debacie nad Sprawozdaniem z realizacji Narodowego Programu Zwalczania Chorób Nowotworowych przedstawionym w dniu 12 września 2014 roku w trakcie posiedzenia sejmowej komisji zdrowia, poseł Czesław Hoc (PiS) wskazał na konieczność refundacji badań genetycznych w kontekście obniżania zachorowalności i wczesnego wykrywania raka [6].
Próbka została wysłana do zbadania do niemieckiego laboratorium
czyli o jakości i certyfikacji badań molekularnych w Polsce
Po przeprowadzeniu wywiadu Profesor powiedział, że podejrzewa niedrobnokomórkowego raka płuc z dodatnią mutacją w genie ALK. Oczywiście wcześniej próbki węzłów badane były też pod kątem mutacji w tym genie, ale wszystkie wyniki były negatywne. Profesor Dziadziuszko wiedziony ogromną wiedzą i doświadczeniem, mimo wszystko skierował mnie na oddział w Gdańsku, gdzie lekarze po spuszczeniu płynu z jamy opłucnej, pobrali fragment kolejnego węzła do badania pod kątem obecności mutacji. Próbka została wysłana do zbadania do niemieckiego laboratorium (oczywiście dzięki Profesorowi). W oczekiwaniu na wynik z Niemiec przyjęłam jeszcze 3 kursy chemii w szpitalu w Elblągu. W sierpniu 2013 roku otrzymaliśmy wynik z Niemiec – pozytywny. Od profesora Dziadziuszko dowiedzieliśmy się, że dzięki temu jest się możliwość terapii inhibitorem ALK. Profesor obiecał pomóc w jej przeprowadzeniu i dotrzymał słowa. Terapia dała natychmiastowe efekty, minęły wszystkie odczuwane dolegliwości. Bóle kości przestałam odczuwać w ciągu 2 tygodni. Czułam ogromną radość [7] – to fragment historii Basi, który niech będzie przyczynkiem do rozważań na temat kolejnego problemu – jakości badań molekularnych w Polsce w zakresie onkologii.
Kilka lat temu duże wrażenie wywarła na mnie prezentacja wygłoszona na międzynarodowej konferencji. Przedstawicielka Francji – państwa w którym terapia nowotworów jest na jednym z najwyższych w Europie poziomie – przedstawiła działający w tym kraju regionalny system certyfikowanych laboratoriów diagnostyki molekularnej. Na podstawie przeprowadzonych przez nie badań genetycznych wdraża się u pacjentów onkologicznych możliwie najlepsze dostępne leczenie celowane. Jest to z korzyścią zarówno dla pacjenta, którego organizm nie jest osłabiony skutkami ubocznymi wyczerpującej chemioterapii, jak i dla systemu.
Koszty wprowadzenia od razu terapii spersonalizowanej są niższe niż leczenie najpierw chemioterapeutykami, a później lekami celowanymi. Poza tym wiadomo, że w terapii nowotworów trzeba zacząć od podania najefektywniej działających leków w pierwszej linii. Ten model leczenia jest najbardziej skuteczny, a nie odwrotne postępowanie – zaczynanie leczenia od często słabo działającej terapeutycznie, za to wyniszczającej chemioterapii, jak to jest w większości obowiązujących u nas standardów.
W Polsce też mamy sieć wojewódzkich laboratoriów diagnostyki molekularnej, ale ocena ich działalności przeprowadzona przez organizacje pacjentów onkologicznych na podstawie Sprawozdania Ministerstwa Zdrowia z realizacji Narodowego Programu Zwalczania Chorób Nowotworowych w roku 2013 jest jednoznacznie miażdżąca – Obecny stan diagnostyki genetycznej w onkologii opiera się w dużej mierze na podwykonawstwie prowadzonym dla szpitali posiadających umowy z NFZ na realizację świadczeń zdrowotnych. Implikacją takiego stanu jest to, że na bazie wyniku badania przeprowadzonego w laboratorium diagnostyki genetycznej nie posiadającym żadnych akredytacji i weryfikacji przez nadzór merytoryczny, lekarz podejmuje decyzję o dalszym postępowaniu z chorym.
Wniosek z tej oceny, jak i z postulatów organizacji pacjentów do NPZChN na lata 2016- 2025 jest następujący: Wobec braku procesu certyfikacji laboratoriów, braku realnego monitorowania oraz nadzoru testów wykorzystywanych w takich laboratoriach rekomendujemy powołanie centralnego ośrodka onkologicznego diagnostyki genetycznej, którego funkcjonowanie może zoptymalizować proces kwalifikacji chorych do terapii oraz poprawić wyniki leczenia [8].
Stanowisko pacjentów popiera Krajowy Konsultant w dziedzinie onkologii Klinicznej, prof. Maciej Krzakowski – Konieczne jest również stworzenie prawidłowego systemu prowadzenia badań molekularnych chorych na nowotwory (…). W pojęciu prawidłowości systemu mieści się zapewnienie odpowiedniej jakości wykonywania badań oraz właściwego finansowania [9].
Około 100 000 kobiet ma mutacje w genach BRCA1 i BRCA2
czyli o roli diagnostyki genetycznej w profilaktyce nowotworów
Diagnostyka molekularna w onkologii, to nie tylko określanie mutacji genu u pacjenta w celu wdrożenia leczenia nowoczesną terapią, to przede wszystkim profilaktyka i prewencja chorób nowotworowych. Co w Polsce robi się w tym zakresie?
Otóż mamy – Program Opieki nad Rodzinami Wysokiego Dziedzicznie Uwarunkowanego Ryzyka Zachorowania na Nowotwory Złośliwe koordynowany przez Ministerstwo Zdrowia w ramach Narodowego Programu Zwalczania Chorób Nowotworowych. Niestety dotyczy on tylko dwóch modułów: – wczesnego wykrywania nowotworów złośliwych w rodzinach wysokiego dziedzicznie uwarunkowanego ryzyka zachorowania na raka piersi i raka jajnika oraz wczesnego wykrywania i prewencji nowotworów złośliwych w rodzinach wysokiego ryzyka zachorowania na raka jelita grubego i błony śluzowej trzonu macicy.
Moduł pierwszy obejmuje grupę kobiet zagrożonych rakiem piersi, które jak Angelina Jolie mają mutację w genie BRCA1, BRCA2. Powinny one zachować szczególną czujność onkologiczną. Ocenia się, że od 10 do 20% zachorowań na raka piersi to osoby z mutacją w genach BRCA1 i BRCA2. W Polsce, według niektórych szacunków, około 100 000 kobiet ma mutacje w genach BRCA1 i BRCA2. Około 20% zachorowań na raka jajnika dotyka nosicielek tych mutacji. Od 10 do 15% przypadków tego najczęstszego u kobiet nowotworu ma postać rodzinną. Podstawą do wyłonienia pacjentek z grupy wysokiego ryzyka dziedzicznie uwarunkowanego raka piersi i jajnika jest wywiad rodzinny. Ustala się w nim występowanie nowotworu w rodzinie i wiek zachorowania. Wywiad obejmuje krewnych I i II stopnia.
Wskazania do wykonania badania mutacji w genie BRCA obejmują:
- co najmniej 2-3 przypadki raka piersi w rodzinie, zwłaszcza rozpoznanych przed 50. rokiem życia;
- diagnozę w rodzinie przypadków raka piersi w postaci rdzeniastej, bez receptorów estrogenowych;
- rodzinnie występujący rak jajnika,
- diagnozę przypadków nietypowych postaci raka piersi, zwłaszcza rak obustronny, wczesny, przed 40 rokiem życia,
- rak piersi u mężczyzny w rodzinie
- potwierdzoną obecność mutacji BRCA1, BRCA2 w rodzinie.
W zakresie diagnostyki molekularnej raka piersi możemy się pochwalić ośrodkiem o światowej randze, jakim jest Międzynarodowe Centrum Nowotworów Dziedzicznych Pomorskiego Uniwersytetu w Szczecinie, którym kieruje prof. dr hab. n. med. Jan Lubiński. Ostatnim osiągnięciem tej placówki, o którym już głośno – jest wyodrębnienie nowej mutacji genu raka piersi RECQL. Podobno nie jest ona tak groźna jak BRCA1, BRCA2. Już na tym przykładzie widać, jak dynamicznie rozwija się obecnie medycyna molekularna, dając nadzieję chorym.
Drugi moduł bezpłatnych testów genetycznych wykonywanych w ramach Programu Opieki Nad Rodzinami Wysokiego Dziedzicznie Uwarunkowanego Ryzyka Zachorowania Na Nowotwory Złośliwe, dotyczy osób z podejrzeniem dziedzicznego raka jelita grubego. Jest to: zespół Lyncha I – występowanie tylko raka jelita grubego oraz zespół Lyncha II – występowanie raka okrężnicy oraz innych m.in. raka trzonu macicy, piersi, żołądka, jelita cienkiego, wątroby, dróg żółciowych oraz dróg moczowych, a także chłoniaków. Wskazaniem do wykonania testów w kierunku wykrycia mutacji genów, będących przyczyną dziedzicznego raka jelita grubego są tzw. kryteria amsterdamskie ustalane na podstawie wywiadu rodzinnego, czyli: występowanie w rodzinie co najmniej trzech przypadków raka jelita grubego wśród krewnych pierwszego stopnia, co najmniej w dwóch generacjach i przynajmniej jeden przypadek tego nowotworu w młodym wieku(<50 lat).
W zależności od tego, jaką nieprawidłową mutację genu wykryto testem, ich nosiciele powinni zrobić określone badania diagnostyczne. Może to być np.: kolonoskopia, mammografia, USG piersi, rezonans piersi, badanie ginekologiczna, badanie poziomu Ca125. Oprócz profilaktyki możliwa jest także np. chemioprewencja, czyli zapobiegawcze zażywanie leków zmniejszających ryzyko zachorowania. W szczególnych przypadkach pacjenci mogą zdecydować się na usunięcie narażonego organu, tak jak to zrobiła Angelina Jolie, ale to już temat na osobny artykuł. Przede wszystkim powinni przestrzegać zasad zdrowego stylu życia, aby nie stymulować poza genetycznych czynników uaktywniających mutację genów oraz przestrzegać zaleceń dla osób z wysokim ryzkiem zachorowania na te nowotwory.
Program Opieki nad Rodzinami Wysokiego Dziedzicznie Uwarunkowanego Ryzyka Zachorowania na Nowotwory jest realizowany przez specjalistyczne poradnie genetyczne działające w całej Polsce. Placówki te w ramach świadczeń NFZ zapewniają bezpłatną konsultację pacjentów z podejrzeniem dziedzicznej predyspozycji do zachorowania na nowotwory złośliwe, na podstawie skierowań lekarskich wystawionych przez lekarzy onkologów lub lekarzy podstawowej opieki zdrowotnej. Wskazania do konsultacji genetycznej mają przede wszystkim osoby, u których rozpoznano raka w młodym wieku, z obciążonymi wywiadami rodzinnymi w kierunku nowotworów złośliwych.
Przykładowo zachorowanie na: raka jajnika; rdzeniastego raka tarczycy; raka piersi receptorowo ujemnego/potrójnie negatywnego w dowolnym wieku; raka piersi przed 50 rokiem życia; obustronnego raka piersi; raka piersi u osoby, która posiada przynajmniej jedną krewną, u której rozpoznano raka jajnika lub na raka piersi; raka piersi u mężczyzny; białaczkę, mięsaka, nowotwór ośrodkowego układu nerwowego przed 45 rokiem życia; raka nerki przed 45 rokiem życia; raka jelita grubego przed 50 rokiem życia; raka błony śluzowej trzonu macicy przed 50 rokiem życia; nowotwór ze spektrum zespołu Lyncha o ile w rodzinie są bliscy krewni, u których rak jelita grubego lub inne nowotwory ze spektrum zespołu Lyncha wystąpiły w młodym wieku, a także rozpoznanie u pacjenta mnogich polipów w jelicie grubym
U zdrowych osób konsultacja genetyczna jest uzasadniona, gdy jest znana mutacja markerowa, odpowiedzialna za zachorowania na nowotwory złośliwe w rodzinie [11].
Jak widać NFZ nie refunduje badań genetycznych, czy choćby konsultacji w tym zakresie u pacjentów z zachorowaniem na inne rodzajów nowotworów, u których w przypadku wykrycia określonej mutacji można zastosować leczenie celowane, jak np. w czerniaku w zaawansowanym, przerzutowym stadium, gdzie przy obecności mutacji BRAF, od 2013 roku chorzy mają dostęp do leczenia wemurafenibem. Innym przykładem jest niedrobnokomórkwy raka płuca, gdzie mutacje aktywujące genu EGFR oraz rearanżacje genu ALK, sygnalizują potencjalną wrażliwość nowotworu na nowoczesne leki z grupy inhibitorów kinazy tyrozynowej genu EGFR (TKI EGFR) (erlotynib, gefitynib, afatynib) lub inhibitor kinazy tyrozynowej genu ALK ( kryzotynib).
Pisząc o dziedzicznie uwarunkowanych nowotworach trzeba wspomnieć o związanych z nimi problemach społeczno-obyczajowych. W wielu, głównie małych środowiskach, rak nadal jest tematem, o który się nie mówi. Dotyczy to przede wszystkim nowotworów stref intymnych – raka piersi, trzonu macicy, jajników u kobiet, czy prostaty u mężczyzn, nowotworów sromu, czy odbytu u obu płci. Także raka jelita grubego, zwłaszcza, kiedy wyłoniona jest stomia. W małych miejscowościach, gdzie wszyscy się znają, bywa że ukrywa się nawet przed rodziną fakt zachorowania na ten rodzaj nowotworu. A jest to dla krewnych chorego często informacja o życiowym znaczeniu. Personel medyczny – lekarze, pielęgniarki, psycholodzy – jest z racji zawodowych zobowiązany do uświadomienia pacjentowi konieczności przekazania krewnym wiedzy o dziedzicznym podłożu choroby. Wiąże się to często z potrzebą wykonania odpowiedniego badania genetycznego. Ogromną rolę w zakresie przełamywania tabu, jak i profilaktyki chorób nowotworowych odgrywają organizacje pacjentów takie jak Amazonki, Gladiator, Pol-ilko, Magnolia. Nikt lepiej niż pacjent, który przeszedł doświadczenie choroby nie przekaże innym wiedzy o niej, ostrzeże przed ryzykiem zachorowania, zachęci do działań profilaktycznych, w tym wykonania testów molekularnych.
W tym czasie guz w śródpiersiu rósł
czyli diagnostyka molekularna w przypadku nowotworów rzadkich
Refundacji badania genetycznego kierunku mutacji w genach BRCA1, BRCA2 jest niewątpliwą zasługą Amazonek, które jako największa i najbardziej skutecznie działająca organizacja pacjentów z nowotworami, wywalczyły dla polskich kobiet dostęp do bezpłatnego wykonywanie tego badania przy określonych wskazaniach. Takich możliwości nacisku na decydentów nie ma niestety większość grup pacjentów onkologicznych. Dotyczy to zwłaszcza liczących niewiele osób grup chory na nowotwory rzadkie, które nie są często zorganizowane w fundacje czy stowarzyszenia. W przypadku tych pacjentów droga do diagnozy jest zwykle trudna, zbyt długa i kosztowna, a pamiętajmy, że tych grup chorych będzie przybywać w miarę rozpoznawania nowych mutacji genów.
W tej chwili trwają dyskusje o sensowności szybkiej terapii onkologicznej, dzięki której pacjent będzie miał postawioną diagnozę w ciągu 9 tygodni. W moim przypadku od pierwszych objawów choroby w kwietniu 2010 roku, z którymi zgłosiłam się do lekarza, do postawienia w marcu 2011 roku diagnozy – ziarnica złośliwa (chłoniak Hodgkina) minął aż rok. W tym czasie guz w śródpiersiu rósł [12] – pisze Marzena Erm (27 lat). Przez prawie rok walczyła ze świądem, alergią, nerwicą, jesiennym przeziębieniem przeszła kilka badań diagnostycznych, a w jej przypadku zdaniem prof. dr hab. n. med. Jerzego Hołowieckiego z Centrum Onkologii w Gliwicach – Biopsja igłowa nie dostarcza materiału wystarczającego do dokładnego rozpoznania i niepotrzebnie wydłuża czas do rozpoznania. W różnicowaniu z innymi chłoniakami istotne są badana immunohistochemiczne (…). Badania obrazowe USG, RTG, CT, PET/CT i biopsja szpiku są potrzebne do oceny rozległości zmian, czyli tzw. „stagingu”, pomagają też w wyborze miejsca pobrania wycinka do badania histopatologicznego [13].
Podobnie, jak u Marzeny wyglądało postawienie diagnozy u Rafała, Basi i Pani Jadwigi Szuster – Po 10 latach zmieniłam lekarza i to był ostatni moment na przeprowadzenie pogłębionej diagnostyki. Czułam się coraz gorzej, zaczęła mi przeszkadzać śledziona i wątroba. Zgłaszałam te dolegliwości przy każdej wizycie u hematologa, ale słyszałam, że muszę się z tym pogodzić, ponieważ w czerwienicy tak jest. Prosiłam o zmianę leku, ale też słyszałam, iż jest on odpowiedni. Wreszcie po długo wyczekiwanej wizycie w klinice hematologicznej na Śląsku, kompleksowe badania wykazały, że choroba jest bardzo zaawansowana. Dowiedziałam się, że jest to mielofibroza. Nigdy nie przypuszczałam, że znajdę się w gronie „wybrańców” losu, którzy mają tak rzadką chorobę, bo na mielofibrozę w Polsce choruje zaledwie tysiąc osób [14].
Ci „wybrańcy” losu czasami przez wiele miesięcy, a nawet lat – jak w przypadku Pani Janiny – zmagają się ze skutkami nierozpoznanej lub źle zdiagnozowanej choroby. Jak pisze Pani Janina żyją dzięki swojemu uporowi i dobremu lekarzowi lub jak Rafał czy Marzena stają się managerem własnego losu. Dzięki wsparciu przyjaciół, rodziny, znajomych – a także zupełnie nieznanych, ale życzliwych ludzi – gromadzą pieniądze na leczenie z wykorzystaniem nowoczesnych terapii celowanych, których podstawą jest diagnostyka molekularna. To grupy „pacjentów wykluczonych”, o których los nikt nie dba. Ich głos jest zbyt słaby, by dodarł do osób odpowiedzialnych za zdrowie w naszym kraju. Problemy z diagnostyką i leczeniem tych pacjentów rozwiązałby z pewnością publiczna placówka, taka jak serwis terapii spersonalizowanej prowadzonej przez niemiecko-węgiersko firmę [2], bo na usługi tej znakomicie działającej firmy stać nielicznych chorych onkologicznie Polsce. Pytaniem jest to też, czy warto wyważać otwarte drzwi i zamiast tworzyć od podstaw taki ośrodek, nie byłoby łatwiej skorzystać z usług wspomnianego serwisu na zasadzie umów z NFZ. Gdyby obie strony widziałaby możliwości takiej współpracy, dla pacjentów z nowotworami sierocymi, byłaby to bardzo korzystne.
Działalność serwisu została zaprezentowana i szeroko omówiona podczas zorganizowanej w Poznaniu 7-ej Międzynarodowej Konferencji Współczesnej Onkologii, znanej na arenie międzynarodowej pod nazwą „7th International Conference of Contemporary Oncology: Personalized Cancer Medicine and Big Data Analysis”. Zdaniem dr Janusza Kocika, dyrektora Wojskowego Instytutu Higieny i Epidemiologii – z zastosowania wielogenowej diagnostyki molekularnej oraz rozwiązań bioinformatycznych potencjalnie mogą skorzystać ci pacjenci, u których niewiele wiadomo na temat dostępnych opcji leczenia, czyli osoby z tak zwanymi „sierocymi” (rzadko występującymi) nowotworami. Inny profil beneficjenta to pacjent, który został przeleczony wszystkimi dostępnymi metodami o udokumentowanej wiarygodności i cały czas jest w stanie i ma wolę, żeby leczyć się dalej. Informacja może wnieść do procesu decyzyjnego nową jakość, gdy istnieje wiele opcji leczenia farmakologicznego, a tę spersonalizowaną wybiera się dostosowując ją do stanu pacjenta, chorób współistniejących i spodziewanych objawów bocznych, a także – niestety – do sytuacji socjoekonomicznej [15].
Zmniejsza odsetek nieprawidłowo leczonych chorych
czyli o znaczeniu diagnostyki molekularnej w skuteczność leczenia pacjentów z nowotworami
Niewątpliwe jest znaczenie wspomnianych badań, ponieważ zastosowanie leczenia dostosowanego do charakterystyki genetycznej jest bardziej skuteczne i zmniejsza odsetek nieprawidłowo leczonych chorych – stwierdza prof. Maciej Krzakowski [16]. Ta wypowiedź porusza jeszcze jeden aspekt leczenia pacjentów z chorobami nowotworowymi w Polsce, który stał się ostatnio tematem debaty zorganizowanej przez fundację „Alivia” – mała dostępność do nowoczesnych terapii i związana z tym niska liczba osób z pięcioletnim przeżyciem od diagnozy. Pod względem skuteczności leczenia chorych na nowotwory jesteśmy na jednym z ostatnich miejsc w Europie, a bez usystematyzowania sytuacji diagnostyki molekularnej w polskiej onkologii nie mamy szans na wprowadzenie terapii celowanych. Między innymi dostępność do tego leczenia podnosi do blisko 70% liczbę pacjentów onkologicznych z 5-letnimi przeżyciem w Europie Zachodniej, wobec zaledwie 47 % przeżycia pięcioletniego chorych na nowotwory w Polsce. Jak obliczono, w naszym kraju co roku z powodu nowotworów umiera o 30 tys. osób więcej niż państwach europejskich, w których przeżywalność jest najwyższa w Europie. Jest to liczba mieszkańców małego miasteczka. Czy możemy się na to zgodzić?
Coraz bardziej oczywisty jest fakt, że nie ma jednego uniwersalnego leku na raka, ale ważne jest to, iż potrafimy tworzyć coraz bardziej skuteczne, precyzyjnie działające terapie celowane w określone mutacje genów, która są przyczyną nowotworów. Jednak, żeby można było je zastosować trzeba najpierw przeprowadzić badanie genetyczne, które określi cel ataku. Do tego brakuje nam patologów, certyfikacji, ustaleń prawnych i finansowych rozwiązań, a także centralnego ośrodka onkologicznego diagnostyki genetycznej. Konieczne jest także współdziałanie w tym zakresie wszystkich zainteresowanych stron: pacjentów, lekarzy onkologów, patomorfologów i decydentów, a także wsparcie polityków. Aby skutecznie leczyć pacjentów z nowotworami w Polsce za pomocą nowoczesnych terapii musimy najpierw stworzyć jej podstawy, czyli właściwie działający system onkologicznej diagnostyki molekularnej. Aktualna sytuacja w polskiej onkologii w tym zakresie wygląda jak w znanej anegdocie o Napoleonie, na którego cześć nie oddano salw powitalnych w pewnym miasteczku, bo jak tłumaczył się miejscowy burmistrz: Powodów jest ze dwadzieścia. Po pierwsze nie mamy armat. Dziękuję – odpowiedział cesarz – pierwszy wystarczy.
PRZEJDŹ DO: DIAGNOSTYKA MOLEKULARNA NOWOTWORÓW