9 sierpnia 2021 roku Prezes Agencji Oceny Technologii Medycznych i Taryfikacji wydał negatywną opinię w sprawie objęcia refundacją leku Reblozyl (luspatercept) w ramach programu lekowego „Leczenie dorosłych pacjentów z niedokrwistością zależną od transfuzji z powodu zespołów mielodysplastycznych o ryzyku bardzo niskim, niskim i pośrednim z obecnością pierścieniowatych syderoblastów, u których wystąpiła niedostateczna odpowiedź na leczenie erytropoetyną, lub którzy nie kwalifikują się do takiego leczenia (ICD-10 D46.1)”.
Brak rekomendacji Prezesa AOTMiT jest oparty na przesłankach ekonomicznych i nie kwestionuje udowodnionej skuteczności klinicznej leku. Niestety negatywna opinia Prezesa AOTMiT, choć nie przekreśla szansy na refundację Reblozylu, to całkowicie zamyka możliwość stosowania leku w ramach RDTL w tym wskazaniu.
– Luspatercept to wielki przełom w medycynie, gdyż zmniejsza zapotrzebowanie na transfuzje krwi pacjentów od nich uzależnionych. Regularne przetoczenia są obarczone uciążliwymi i groźnymi dla zdrowia konsekwencjami. Prowadzą do obciążenia żelazem, którego nadmiar trzeba usuwać z organizmu, by nie uszkodził organów wewnętrznych takich jak wątroba, serce, śledziona, wywołują reakcje alergiczne oraz infekcje. Rytm życia wyznaczają wizyty w szpitalu, utrudniając, a nawet uniemożliwiając codzienne funkcjonowanie. Rozmawiałam z pacjentami, którzy przyjmują luspatercept i wiem, jak ta terapia odmieniła ich życie. Mamy świadomość, że lek wciąż znajduje się w procesie refundacji, ale niepokoi nas fakt, że nie jest już osiągalny w ramach procedury ratunkowego dostępu (RDTL), a jak wiemy refundacja trwa średnio 2 lata i przez ten czas kolejni pacjenci nie będą mieli możliwości skorzystania z tej terapii – komentuje Aleksandra Rudnicka, Rzecznik Polskiej Koalicji Pacjentów Onkologicznych.
Terapia ta jest także niezwykle ważna w kontekście gospodarowania zasobami krwi w Polsce, które mają kluczowe znaczenie dla sprawnego funkcjonowania systemu ochrony zdrowia. Zapotrzebowanie na przetoczenia składników krwi rośnie wraz ze starzeniem się populacji i postępem medycyny, zwłaszczaw transplantologii, onkologii, hematologii, chirurgii sercowo-naczyniowej.
Obecnie około 2/3 zasobów krwi jest wykorzystywana w leczeniu chorób przewlekłych. Hematolodzy i transfuzjolodzy są zgodni, że w perspektywie najbliższych lat będziemy musieli się mierzyć z jej deficytem.
– Luspatercept daje dobre efekty leczenia chorych z niedokrwistością zależną od transfuzji u pacjentów z zespołami mielodysplastycznymi z obecnością pierścieniowatych syderoblastów. Stosowanie go powoduje średnie zmniejszenie zużycia KKCz o ok. 21%, co przekłada się na osiem jednostek KKCz rocznie na pacjenta, a to jest oszczędność aż czterech litrów krwi. To realna korzyść dla pacjentów, którzy docelowo uniezależniają się od przetoczeń i nie wymagają hospitalizacji. Dzięki procedurze RDTL do tej pory skorzystało z terapii ok. 10 pacjentów i to jest to bardzo pozytywny bodziec do leczenia tym lekiem kolejnych chorych – tłumaczy dr Bożena Katarzyna Budziszewska, Konsultant Wojewódzki w dziedzinie hematologii dla województwa mazowieckiego, Członek Zarządu PTHiT, Kierownik Oddziału Diagnostyki Hematologicznej Kliniki Hematologii IHiT.
Luspatercept
Luspatercept-aamt jest pierwszym w swojej klasie lekiem zwiększającym dojrzewanie komórek erytroidalnych w procesie erytropoezy, wspomagającym końcowy etap dojrzewania erytrocytów, co wykazano w modelach zwierzęcych.
Luspatercept jest obecnie zarejestrowany w Stanach Zjednoczonych w leczeniu:
- niedokrwistości u dorosłych pacjentów z beta-talasemią wymagających regularnych przetoczeń krwinek czerwonych oraz
- niedokrwistości opornej na lek pobudzający erytropoezę, wymagającej przetaczania 2 lub więcej jednostek krwinek czerwonych w okresie 8 tygodni u dorosłych pacjentów z zespołami mielodysplastycznymi z pierścieniowymi syderoblastami (MDS-RS) oraz nowotworami mielodysplastycznymi/mieloproliferacyjnymi z pierścieniowymi syderoblastami i trombocytozą (MDS/MPN-RS-T) ryzyka od bardzo niskiego do pośredniego.
W ostatnich dniach czerwca 2020 roku Komisja Europejska zarejestrowała luspatercept w leczeniu wymagającej przetoczeń niedokrwistości u dorosłych pacjentów z zespołami mielodysplastycznymi (MDS) lub beta-talasemią. Zespoły mielodysplastyczne (MDS) to grupa rzadkich nowotworowych chorób krwi.
Luspatercept reguluje końcowy etap dojrzewania erytrocytów i może potencjalnie ograniczyć lub całkowicie wyeliminować potrzebę wykonywania regularnych przetoczeń krwinek czerwonych. Lek umożliwia pacjentom zastąpienie przetoczeń krwi farmakoterapią w postaci tabletek, co istotnie wpływa na komfort leczenia oraz jakość ich życia.
Decyzja Komisji Europejskiej została podjęta na podstawie danych pochodzących z badań klinicznych MEDALIST i BELIEVE, które oceniały bezpieczeństwo i skuteczność luspaterceptu w leczeniu niedokrwistości związanej z zespołami mielodysplastycznymi oraz u chorych z z beta-talasemią.
Dane z badania MEDALIST wykazały istotną statystycznie poprawę w zakresie zmniejszenia częstości przetoczeń krwinek czerwonych przy zastosowaniu luspaterceptu, co stanowiło pierwszorzędowy punkt końcowy badania: u 37,9% pacjentów, którym podano luspatercept, osiągnięto uniezależnienie od przetoczeń krwinek czerwonych na co najmniej osiem tygodni w ciągu pierwszych 24 tygodni badania, vs. 13,2% pacjentów otrzymujących placebo.
Badanie spełniło również drugorzędowy punkt końcowy w postaci uniezależnienia od przetoczeń na co najmniej 12 tygodni w ciągu pierwszych 24 i 48 tygodni badania, które uzyskano u znacznie wyższego odsetka pacjentów przyjmujących luspatercept niż placebo.
Wyniki badania MEDALIST zaprezentowano po raz pierwszy podczas sesji plenarnej corocznej konferencji Amerykańskiego Towarzystwa Hematologii (ASH) w 2018 roku, gdzie doniesienie otrzymało nominację jako Best of ASH.
Zespoły mielodysplastyczne
Zespoły mielodysplastyczne (MDS) to grupa rzadkich nowotworowych chorób krwi, które cechuje nieskuteczne wytwarzanie przez organizm zdrowych krwinek czerwonych, krwinek białych oraz płytek krwi. W efekcie, zespoły mielodysplastyczne mogą prowadzić u chorych do rozwoju niedokrwistości, groźnych zakażeń, a także progresji do ostrej białaczki szpikowej (AML).
Wielu chorych na MDS, u których wystąpi niedokrwistość, wymaga regularnych przetoczeń krwi w celu zwiększenia liczby zdrowych krwinek czerwonych w krwiobiegu. Z częstymi przetoczeniami krwi związane jest zwiększone ryzyko niepożądanych reakcji poprzetoczeniowych, zakażeń oraz przeładowania organizmu żelazem.
Zarejestrowany przez Komisję Europejską luspatercept umożliwia chorym zastąpienie uciążliwych transfuzji krwi farmakoterapią w postaci tabletek.
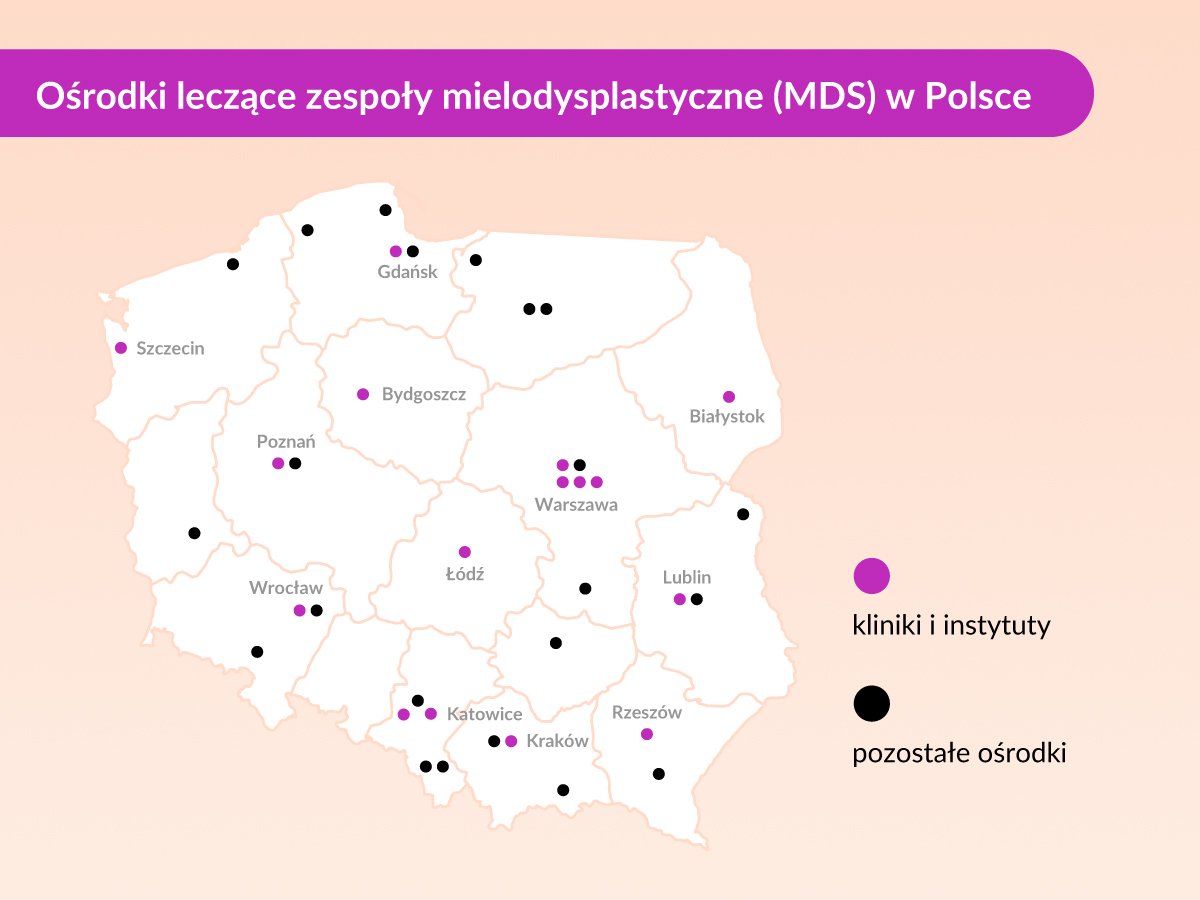
Lista ośrodków leczących zespoły mielodysplastyczne w Polsce
Sprawdź listę ośrodków (Kliniki i Instytuty) na terenie naszego kraju, które leczą zespoły mielodysplastyczne.
PRZEJDŹ DO: HEMATOONKOLOGIA




















Proszę o informację. Jaki jest koszt tego leku. 1 kuracji. I czy lek ten jest dostępny w Polsce, w aptekach.
Moja mama potrzebuje tego leku.Ma przetoczenia co 2-3 tygodnie.PROSZE
Witam.
Czy jest szansa aby skorzystać z tej kuracji. Ewentualnie jaki jest koszt takiej kuracji prywatnie?
Jaki jest koszt tej terapi.Czy jest to lek refundowany?
Hematolodzy go niechca stosowac