Terapia celowana molekularnie raka (personalizowana) stanowi nową i obiecującą formę terapii onkologicznej, z którą wiąże się współcześnie szczególne nadzieje w zakresie poprawy skuteczności leczenia antynowotworowego oraz wydłużenia długości całkowitego przeżycia u pacjentów z rozpoznaniem procesu rozrostowego raka.
Dzięki dynamicznemu rozwojowi genetyki, rośnie poziom wiedzy o biologii nowotworów. Odkrywane są specyficzne zaburzenia genetyczne będące przyczyną poszczególnych nowotworów. Badania nastawione są na poszukiwanie leków celujących bezpośrednio w zmianę genetyczną.
Terapia celowana molekularnie, zwana personalizowaną, przyczyniła się do ogromnego postępu w leczeniu nowotworów złośliwych.
Warto pamiętać, że zastosowanie leku celowanego molekularnie wymaga określenia, czy u danego pacjenta występuje zaburzenie, na które lek działa (tzw. cel molekularny). Niezbędne jest wykorzystanie do tego wysoce specjalistycznych testów molekularnych.
Terapia celowana molekularnie to forma leczenia nowotworów zaliczana potocznie do chemioterapii (leczenia systemowego), choć używa się w niej leków, które nie są typowymi cytostatykami. Jest ona oparta na lekach planowanych molekularnie, czyli takich, które wykorzystują swoiste mechanizmy komórkowe, blokując te mechanizmy albo receptory komórek nowotworowych.
Leczenie celowane nowotworów wpisuje się w ramy tzw. medycyny personalizowanej, a więc takiej, która oparta jest na znajomości patogenezy molekularnej zmian u pojedynczego pacjenta, co pozwala na optymalizację i indywidualizację leczenia. Wiedza ta pozwala na dostosowanie i zastosowanie terapii celowanej, ukierunkowanej na zablokowanie kluczowego mechanizmu w rozwoju choroby.
SPRAWDŹ: ONKOLOGIA PRECYZYJNA
Terapia celowana molekularnie
Wielu ekspertów uważa, że przyszłością leczenia nowotworów jest TERAPIA CELOWANA MOLEKULARNIE, czyli stosowanie leku skierowanego bezpośrednio przeciw komórce nowotworowej z określoną zmianą genetyczną. Leczenie spersonalizowane jest skuteczne, pod warunkiem, że w komórce nowotworu danego pacjenta znajduje się CEL MOLEKULARNY. Tym celem jest konkretnie zmieniony gen/białko powstałe na matrycy nieprawidłowego genu.
Nawet najlepszy lek i terapia celowana molekularnie nie będą skuteczne, jeśli nie znajdziemy dla nich u danego pacjenta celu molekularnego.
Z tego względu niezbędnym warunkiem powodzenia terapii celowanej jest wnikliwa ocena genetyczna komórek nowotworu i określenie przewidywanej podatności pacjenta na konkretne leczenie.
Leczenie personalizowane raka
Prawidłowe komórki cechuje równowaga metaboliczna. Oznacza to, że wszystkie procesy są pod kontrolą. Natomiast w komórkach nowotworowych na skutek zmian w wielu różnych genach ta regulacja zawodzi. Dzięki wieloletnim badaniom naukowców udało się zgromadzić wiedzę i metody, które pozwalają lekarzom wnikać w biologię komórki, próbować sterować nią i przywracać w niej równowagę. To ta wiedza stanowi podstawę terapii nakierowanej na cele molekularne, zwanej też terapią celowaną czyli personalizowaną.
Komórka nowotworowa żyje, więc zachodzą w niej różne procesy metaboliczne, choć – inaczej niż w zdrowych komórkach, dominują te procesy, które ukierunkowane są na niekontrolowane rozmnażanie. W badaniach molekularnych spośród wielu mechanizmów identyfikuje się taki, który w komórkach nowotworowych konkretnego raka jest dominujący. Jeżeli uda się znaleźć odpowiedni lek, który blokuje mechanizm namnażania danego nowotworu, to jest szansa, że zostanie on zniszczony. Niestety, zdarza się, że sprytny nowotwór może wykształcić nowy mechanizm i obejść tę blokadę.
Każda komórka posiada różne receptory, za pomocą których komunikuje się z otoczeniem – innymi komórkami, przestrzenią międzykomórkową czy naczyniami układu krwionośnego. Receptory służą do odbierania różnych sygnałów i bodźców. Komórki nowotworowe są zwyrodniałe i niektórych receptorów mają za dużo albo są one specyficzne. Jeśli wiadomo, że takie receptory istnieją, możliwe jest skonstruowanie leku, który działa wybiórczo tylko na komórki nowotworowe, oszczędzając zdrowe.
Ogólnie mówiąc, zadaniem tych leków jest wybiórcze działanie na komórki nowotworowe, bez wpływu na zdrowe komórki. Dzieje się tak, gdyż terapia celowana molekularnie wykorzystuje cechy genetyczne, które różnią komórki nowotworowe od komórek zdrowych.
ZAJRZYJ: GENEM W RAKA – PROFILOWANIE GENOMOWE
Celowane leczenie nowotworu
Aby móc zastosować terapię celowaną molekularnie (personalizowaną) bada się profil nowotworu za pomocą różnorodnych metod biologii molekularnej. Ocenia się np. ekspresję receptorów na błonie komórkowej, czyli liczbę kanałów, poprzez które wnętrze komórki kontaktuje się ze środowiskiem zewnętrznym. Wysoki poziom ekspresji wskazuje, że nowotwór podlega ogromnemu wpływowi czynników produkowanych przez organizm, np. hormonów i pozwala prognozować, że jeśli zablokuje się te receptory konkretnym lekiem, to chore komórki nowotworowe utracą zdolności życiowe.
Terapia celowana molekularnie jest coraz powszechniej używana – także w Polsce. Niestety również działanie nowoczesnych leków celowanych nie jest wolne od skutków ubocznych. Działania niepożądane są mniejsze niż podczas stosowania klasycznej chemoterapii, ale za to szczególne. Ich toksyczność jest na ogół selektywna i wynika z mechanizmu działania konkretnego preparatu (np. pod wpływem oddziaływania cetuksymabu działającego na receptory naskórkowego czynnika wzrostu, występują odczyny skórne przypominające trądzik.)
Najczęściej stosowanymi lekami ukierunkowanymi molekularnie są monoklonalne przeciwciała (nazwa leku zawiera końcówkę –mab) oraz inhibitory kinaz (nazwa zawiera końcówkę –nib).
Choć z terapią celowaną molekularnie w leczeniu raka wiąże się duże nadzieje, to wiadomo, że dzięki niej można wyleczyć aktualnie tylko niektóre przypadki raka. Dzieje się tak, ponieważ nowotwory są heterogenne – każdy człowiek może mieć swoją własną indywidualną chorobę nowotworową. W praktyce oznacza to, że są chorzy którzy reagują na dany lek w niewielkim stopniu, mimo że u innych pacjentów reakcja była zgodna z oczekiwaną. Zidentyfikowanie osób, które mogą być skutecznie leczone terapią celowaną wymaga przeprowadzenia dodatkowych badań i dużych nakładów finansowych.
Onkologia personalizowana
Aktualnie około 20 markerów predykcyjnych i prognostycznych zostało zaakceptowanych przez Europejskie Towarzystwo Onkologii Medycznej dla raka płuc, żołądka, raka piersi, jelita grubego, raka gruczołu krokowego, jako wystarczająco udokumentowane, aby zostać wprowadzone do praktyki klinicznej.
- leczenie personalizowane raka jelita grubego – w leczeniu przerzutów raka jelita grubego stosowane mogą być przeciwciała monoklonalne skierowane przeciwko receptorowi dla epidermalnego czynnika wzrostu (EGFR) takie jak np. panitumumab czy cetuximat.
- leczenie celowane w czerniaku – w terapii pacjentów z czerniakiem, w którym stwierdzono obecność mutacji aktywującej V600E genu BRAF, lekami z wyboru są inhibitory BRAF np. vemurafenib i dabrafenib.
- terapia celowana w raku podścieliskowym żołądka – w leczeniu podścieliskowego raka żołądka (GIST), zarówno w postaciach z mutacją aktywującą protoonkogenów KIT lub PD-GFRA w komórkach guza, jak i w przypadku braku tych mutacji, standardem terapeutycznym jest stosowanie inhibitora kinazy tyrozynowej – imitinibu.
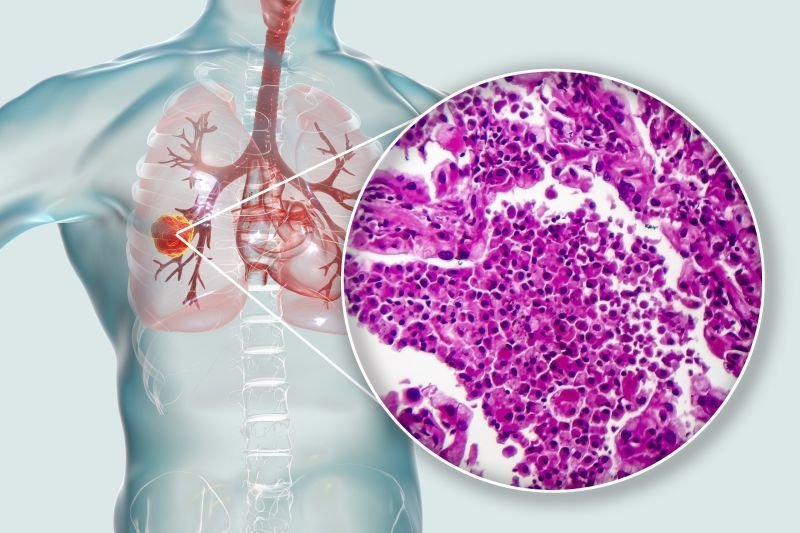
- leczenie personalizowane w raku płuc – rozwój metod leczenia personalizowanego, ukierunkowanego na zahamowanie „wiodącej” molekularnej ścieżki w rozwoju niedrobnokomórowego raka płuc, stał się możliwy dzięki odkryciu obecności mutacji aktywujących w dwóch genach kodujących kinazy tyrozynowe: EGFR oraz gen ALK. W leczeniu pacjentów z niedrobnokomórkowym rakiem płuca, w którego komórkach występuje mutacja aktywująca domenę kinazy tyrozynowej geny BRAF stosuje się gefitinib oraz erlotynib. W przypadku chorych, u których w komórkach guza jest obecna inwersja ramienia krótkiego chromosomu 2 prowadząca do powstania genu fuzyjnego EML4-ALK stosuje się crizotinib.
- leczenie celowane w raku piersi – wprowadzenie zaawansowanych metod diagnostyki molekularnej umożliwiło zidentyfikowanie zmian genetycznych w różnych genach, z różnych ścieżek sygnałowych, co umożliwiło stworzenie klasyfikacji molekularnej raka piersi ( typ: luminalny A, luminalny B, HER-dodatni, potrójnie ujemny TNBC, basal-like oraz TNBC z niską ekspresją klaudyny). Mimo postępu wiedzy o molekularnych podstawach raka piersi, leczenie personalizowane raka sutka oparte jest na ocenie dobrze znanych i szczegółowo opisanych markerów immunohistochemicznych: receptorów estrogenoych, progesteronowych oraz amplifikacji HER2. Obecność receptorów estrogenowych jest kryterium kwalifikacji pacjentek do leczenia hormonalnego (np. tamoxifen, raloxife, letrozol, anastrozol). Amplifikacja HER2, która jest obserwowana u około 20% pacjentek z rakiem piersi, sugeruje, że chore będą reagowały na leki celowane na blokowanie nadekspresji HER2 takie jak trastuzumab (lub herceptyna), lapatinib i pertuzumab.
POLECAMY: IMMUNOTERAPIA NOWOTWORÓW
Skutki uboczne terapii celowanej
Toksyczność skórna
Współczesne leczenie nowotworów składa się trzech metod: chirurgii, radioterapii i leczenia systemowego. Leczenie ogólnoustrojowe bazuje na lekach cytostatycznych, jednakże w ciągu ostatnich dziesięciu lat przewagę zyskuje leczenie terapią celowaną. Oznacza to, że lekarze są w stanie dobrać indywidualną terapię, która w przypadku danego pacjenta będzie najbardziej skuteczna i bezpieczna. Wchodzimy w erę tzw. onkologii personalizowanej, która opiera się na optymalizacji i indywidualizacji leczenia w oparciu o zdefiniowany cel molekularny. Taki rodzaj leczenia jest korzystniejszy dla pacjenta, ponieważ niszczy jedynie komórki nowotworowe. Niestety, również terapia celowana molekularnie wywołuje pewne niepożądane działania uboczne.
O ile działanie klasycznej chemioterapii polega na niszczeniu populacji szybko dzielących się komórek danego typu nowotworu niezależnie od ich profilu molekularnego, to leki molekularne działają tylko na określone grupy komórek, w których występują charakterystyczne zaburzenia molekularne. Z różnic w mechanizmie działania wynika odmienny charakter działań niepożądanych chemioterapii i leków ukierunkowanych molekularnie.
W przypadku terapii celowanej rodzaj objawów ubocznych zależy od typu komórek, na które działa dany lek. Są to najczęściej problemy skórne w postaci: wysypki, zaczerwienienia na skórze dłoni i stóp, ropnych i trądzikopodobnych zmian skórnych czy nadmiernej suchości skóry.
Do tego dochodzą zmiany na paznokciach i skórze wokół nich, blaknięcie skóry czy wypadanie włosów. Problemy ze skórą będące skutkiem ubocznym terapii celowanej mają charakter zróżnicowany – od łagodnych, do wyjątkowo uciążliwych. Zdarza się, że ze względu na wysoki stopień ich występowania oraz istotne obniżenie jakości życia pacjenta, lekarz prowadzący zmuszony jest wstrzymać leczenie.
Szczególnie nasilone powikłania po terapii celowanej obserwuje się u pacjentów poddawanych leczeniu przeciwciałami skierowanymi przeciwko receptorowi dla czynnika wzrostu naskórka EGFR. W warunkach fizjologii EGFR odpowiada za proliferację, dojrzewanie i różnicowanie kolejnych warstw nabłonka. Jego ekspresję potwierdzono zarówno na powierzchni komórek nowotworowych, jak i w zdrowych tkankach organizmu. Obserwacje kliniczne dowodzą, że stosowanie inhibitorów EGFR jest źródłem atrofii skóry oraz powstawania nacieku zapalnego u nawet 70% pacjentów. Konsekwencją indukcji apoptozy komórek naskórka w połączeniu z aktywacją i napływem komórek zapalnych układu immunologicznego jest nasilenie zmian skórnych, które u pacjentów poddawanych terapii celowanej anty-EGFR najczęściej mają charakter:
- zmian w płytce paznokciowej i zmian okołopaznokciowych
- wysypki
- zmian dotyczących włosów
- świądu
- suchości skóry
- zapalenia mieszków włosowych
- hiperpigmentacji;
- teleangiektazji.
Klinicznie najistotniejszym problemem jest wysypka grudkowo-krostkowa, zwana również wysypką trądzikopodobną ze względu na wizualne podobieństwo do trądziku. Jej występowanie obserwuje się u około 80% pacjentów. Wysypka pojawia się najczęściej 2-3 dni po rozpoczęciu leczenia inhibitorami anty-EGFR, a szczyt nasilenia objawów obserwuje się po 2-3 tygodniach. Zmiany skórne na skutek terapii celowanej pojawiają się w okolicy twarzy, szyi, tułowia oraz owłosionej skóry głowy. Co ciekawe, w badaniach klinicznych obserwowano, iż u pacjentów, u których wystąpiło znaczne nasilenie dolegliwości i toksyczności skórnej, odpowiedź na zastosowane leczenie celowane anty-EGFR była lepsza.
Jeszcze do niedawna powikłania skórne towarzyszące terapiom ukierunkowanym były często pomijane lub lekceważone jako problem mało istotny klinicznie. Coraz szersze zastosowanie leków ukierunkowanych na cele molekularne spowodowało w ostatnim czasie wzrost zainteresowania toksycznością skórną oraz sposobami jej leczenia. Opracowano szczegółowe algorytmy postępowania w przypadku zmian skórnych u pacjentów poddanych terapii onkologicznej, a terapia toksyczności skórnej będącej następstwem leczenia celowanego stała się elementem codziennej praktyki.
ZOBACZ WIĘCEJ: NOWE METODY LECZENIA RAKA