Jeszcze do niedawna terapia onkologiczna opierała się na uniwersalnych schematach terapeutycznych z wykorzystaniem chemioterapii i radioterapii. Współczesna medycyna pozwala dobrać terapię indywidualnie dla danego pacjenta. Stało się to możliwe dzięki szerokiej analizie genomów nowotworowych, czyli kompletnego zapisu informacji genetycznej oraz zaangażowaniu sztucznej inteligencji. Onkologia staje się coraz bardziej wyrafinowana i spersonalizowana. Czy jesteśmy świadkami zmiany paradygmatu w leczeniu raka?
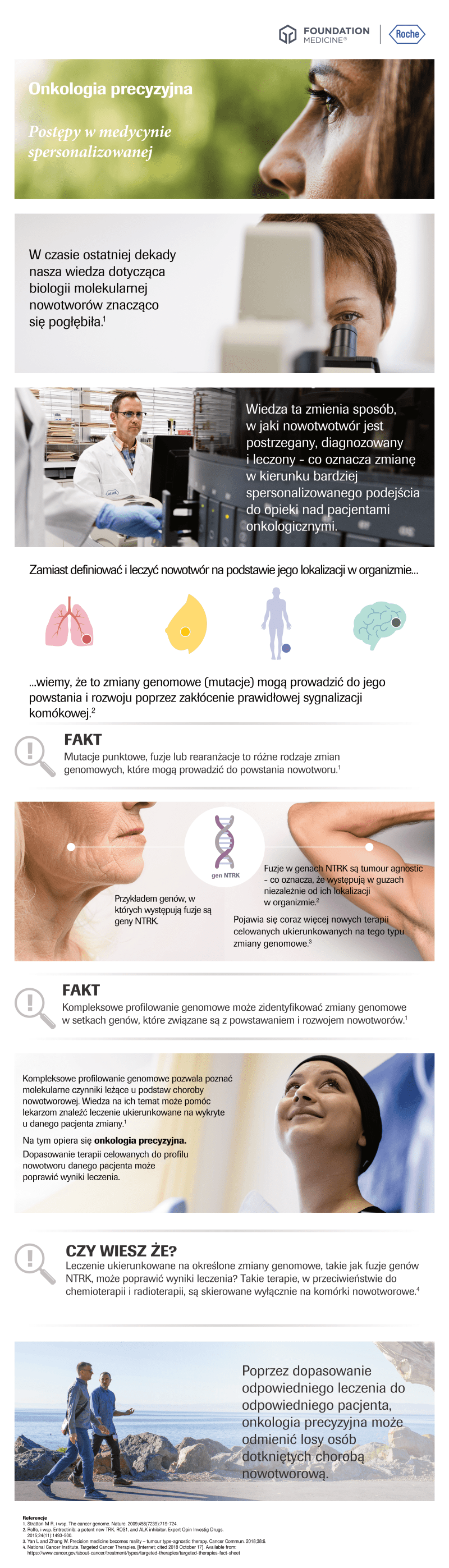
Płuco, pierś, jajnik, jelito, trzustka… Nowotwory od zawsze klasyfikowane były według części ciała oraz narządu, w którym się rozwinęły. Rozwój nowoczesnych technik diagnostycznych, badań genetycznych, molekularnych oraz sztucznej inteligencji (AI) doprowadził do zmiany postrzegania choroby nowotworowej. Jak tłumaczą eksperci, obserwujemy przejście z tzw. onkologii narządowej do onkologii precyzyjnej.
Okazuje się, że guzy, które pod mikroskopem wyglądają identycznie, różnią się od siebie z genomowego punktu widzenia. Co więcej, niektóre rzadkie fuzje genów występują w wielu różnych nowotworach zlokalizowanych w odległych od siebie narządach. Dla przykładu fuzje genów NTRK lub ROS1 mogą dotyczyć mięsaków, potrójnie ujemnego raka piersi, nowotworów głowy i szyi, raka ślinianki, pęcherzyka żółciowego czy raka płuca.
Dynamicznie przyrasta liczba genów i mutacji wykrywanych w guzach nowotworowych, a także leków działających na te mutacje. Badacze są na tropie setek terapii powiązanych z charakterystyką molekularną guzów.
Diagnostyka molekularna guzów nowotworowych staje się niezbędnym elementem procesu diagnostycznego. Wiemy już, że każdy nowotwór posiada swój własny „podpis molekularny”, i może wymagać odrębnego postępowania terapeutycznego.
Co oznacza taka wiedza w praktyce?
Koncepcja tumor-agnostyczna w leczeniu onkologicznym
Leki ukierunkowane na cele molekularne zmieniły podejście w leczeniu wielu typów nowotworów. Jeszcze do niedawna – zgodnie z paradygmatem onkologii narządowej – wspomniane terapie były dedykowane wykrytym mutacjom dla nowotworów zlokalizowanych w konkretnym narządzie.
Tymczasem naukowcy zwracają uwagę na wartość nowego podejścia, które sugeruje, że liczy się przede wszystkim biologia guza, a mniej narząd w którym rozwinęła się choroba. Takie spojrzenie określamy jako koncepcję tumor-agnostyczną.
Przyjmując podejście tumor-agnostyczne wobec choroby nowotworowej, w niektórych przypadkach możliwe staje się rozszerzenie zasięgu terapii personalizowanych i wykorzystanie ich niezależnie od miejsca (narządu), w którym powstał nowotwór.
Przykładem leków ukierunkowanych na czynnik molekularny nowotworu, a nie na lokalizację guza (czyli narząd w którym występuje) są dwa inhbitory TRK w leczeniu chorych na wszystkie nowotwory z fuzją genu NTRK.
– W tym przypadku mówimy o zmianie paradygmatu. A więc nie stosujemy leków w rozpoznaniu określonego typu nowotworu, tylko przy określonej zmianie molekularnej w każdym nowotworze, w którym zostanie ona wykryta. Rearanżacje genów NTRK są faktycznie rzadkie ponieważ w większości nowotworów częstość ich występowania nie przekracza 1%, ale w przypadku stwierdzenia takiej zmiany w badaniu molekularnym na leczenie odpowiada około 80% osób i u większości odpowiedź na leczenie utrzymuje się powyżej roku. Taka fuzja może zostać wykryta w przypadku większości nowotworów, a więc u pacjentów z rozpoznanym rakiem płuca, trzustki, dróg żółciowych, jelita grubego czy czerniakiem. Podobna sytuacja jest w przypadku fuzji genu ROS1. Znamy go z leczenia raka płuca, ale w literaturze opisane są fuzje tego genu u osób z rakiem: jajnika, żołądka, dróg żółciowych, jelita grubego. Innym przykładem są fuzje genu RET. Wykrycie fuzji genów NTRK czy RET w guzie nowotworowym daje dodatkową, skuteczną opcję leczenia – wyjaśnia dr n. med. Marek Szwiec, Kierownik Oddziału Onkologii w Szpitalu Uniwersyteckim im. Karola Marcinkowskiego w Zielonej Górze, ekspert w obszarze genetyki nowotworów.
Diagnostyka molekularna – testy wielogenowe i kompleksowe profilowanie genomowe
Tak jak osoby dotknięte chorobą nowotworową różnią się od siebie, tak każdy profil genomowy nowotworu jest inny. To właśnie on może być kluczem do znalezienia indywidualnej terapii dla każdego pacjenta.
Badanie nowotworu na poziomie molekularnym ma ogromne znaczenie i powinno stanowić pierwszy krok na ścieżce leczenia onkologicznego. Im więcej informacji na temat mutacji występujących w tkance nowotworowej, tym bardziej precyzyjne i personalizowane leczenie.
– Obecnie decyzje terapeutyczne opierają się na badaniu kilku, kilkunastu znanych zmian genomowych w niektórych nowotworach. Przykładem są mutacje RAS i BRAF w raku jelita grubego, mutacje EGFR i geny fuzyjne ALK i ROS1 w raku płuca, mutacje genów BRCA w raku piersi, jajnika, trzustki i raku prostaty. Tak naprawdę posiadamy już testy, które pozwalają wykonać jednocześnie badanie mutacji wielu genów, dają więcej informacji i umożliwiają lepsze dopasowanie leczenia. Określane są one jako testy wielogenowe. Liczba badanych genów jest różna – od kilku do kilkuset. Część testów jest dedykowana dla określonego typu nowotworu, inne mają zastosowanie w przypadku wszystkich nowotworów litych. Celem badania jest znalezienie zmian w genomie napędzających rozwój danego nowotworu. Leki wpływające na zahamowanie ich nadmiernej aktywności dają szansę na długotrwałe odpowiedzi – wyjaśnia dr n. med. Marek Szwiec.
W najbliższej przyszłości możemy spodziewać się wzrostu dostępności testów wielogenowych oraz kompleksowego profilowania genomowego ze względu na postęp technologiczny oraz spadek kosztów takich badań. Profilowanie molekularne guza stanie się elementem codziennej praktyki.
Sztuczna inteligencja w diagnostyce onkologicznej
Zdaniem wielu ekspertów przed nami rewolucja w diagnostyce molekularnej nowotworów. Wielu badaczy, jako jej źródło, wskazuje dynamiczny rozwój sztucznej inteligencji (Artificial Intelligence).
Już dziś AI znajduje praktyczne zastosowanie we wczesnym wykrywaniu niektórych chorób nowotworowych. Największy potencjał sztucznej inteligencji kryje się jednak w możliwości analizy ogromnej ilości danych i sporządzaniu unikalnego „paszportu genomowego” nowotworu.
Bloczek parafinowy zawierający fragment tkanki nowotworowej kryje w sobie bardzo dużą ilość informacji. Niestety, nie wszystkie informacje są dostępne dla oczu. Dlatego naukowcy zwracają się o pomoc do sztucznej inteligencji.
Systemy uczące się typu deep learning przetwarzają ogromne ilości wyników, aby wyłapać korelacje występujące pomiędzy genami, mechanizmami rozwoju oraz strategiami leczenia nowotworów.
Oprogramowanie systemów analizy opartych na sztucznej inteligencji potrafi dostarczyć olbrzymią ilość danych ukrytych w tkance nowotworowej. Otwiera to drogę do zaprojektowania nowych terapii personalizowanych i stanowi fundament, wspomnianej wcześnie, onkologii precyzyjnej.
– Jeżeli chodzi o sztuczną inteligencję to już teraz może być ona wykorzystywana do wczesnego wykrycia raka piersi, raka płuca czy raków skóry. Natomiast wsparcie AI w decyzjach terapeutycznych to przyszłość. Prace nad wykorzystaniem sieci neuronowych do analizy badań całogenomowych nowotworów już trwają. Tutaj nie badamy kilkunastu wybranych genów, ale cały genom. Liczba uzyskanych danych jest ogromna. W analizie tych danych może wesprzeć nas właśnie sztuczna inteligencja. Przed nami badania proteomu i metabolomu guza. Ale im dalej w las, tym więcej drzew – podsumowuje dr n. med. Marek Szwiec, Kierownik Oddziału Onkologii w Szpitalu Uniwersyteckim im. Karola Marcinkowskiego w Zielonej Górze, ekspert w obszarze genetyki nowotworów.
Pojęcie onkologii personalizowanej zyskało właśnie nowe, ważne rozwinięcie. Naukowcy dowiedli, że nowotwór nie jest chorobą konkretnego narządu, ale schorzeniem genomu. Dzięki osiągnięciom diagnostyki molekularnej badacze coraz częściej potrafią precyzyjnie określić mutacje, które odpowiadają za rozwój konkretnego nowotworu.
Otwiera to drzwi do wdrożenia nowych opcji terapeutycznych dopasowanych na podstawie unikalnego „paszportu genomowego” guza i dedykowanych wąskim grupom pacjentów.
Kompleksowe profilowanie genomowe to badanie, które daje szansę chorym na skuteczne i precyzyjne leczenie oparte o podpis molekularny ich nowotworu.
Rozwój onkologii precyzyjnej opartej na koncepcji tumor-agnostycznej otworzył nowy rozdział w walce z rakiem.
Genem w raka. Koncepcja tumor-agnostyczna w leczeniu nowotworów, źródła:
www.magzter.com/article/Business/Newsweek-Europe/Cancer-In-The-Crosshairs
www.roche.pl/pl/roche-polska/foundation-medicine/-zbadajraka.html
www.gene.com/stories/the-next-step-in-personalized-medicine
www.genetyka.bio/sekwencjonowanie-nowej-generacji-w-diagnostyce-medycznej/
Artykuł powstał we współpracy z firmą Roche.
ZOBACZ WIĘCEJ: DZIAŁ ONKOLOGIA PRECYZYJNA