Agencja Badań Medycznych zakwalifikowała do dofinansowania kwotą prawie 8,5 mln zł projekt „Ocena odpowiedzi immunologicznej u chorych leczonych pembrolizumabem z nowo zdiagnozowanym glejakiem wielopostaciowym mózgu (PIRG)” w ramach pierwszego konkursu na realizację niekomercyjnych badań klinicznych.
Badanie realizowane jest pod kierownictwem dr. hab. n. med. Wojciecha Kaspera z Katedry Neurochirurgii i Oddziału Klinicznego Neurochirurgii Wydziału Nauk Medycznych Śląskiego Uniwersytetu Medycznego (ŚUM) w Katowicach.
Projekt ma charakter wieloośrodkowy i obok ŚUM w jego realizację zaangażowany jest Narodowy Instytut Onkologii im. M. Skłodowskiej-Curie Oddział w Gliwicach. Badanie stawia sobie za cel opracowanie nowego schematu leczenia jednej ze skrajnie złośliwych postaci nowotworu mózgu tj. glejaka wielopostaciowego.
ZOBACZ WIĘCEJ: GUZ MÓZGU – OBJAWY
Projekt badawczy dotyczący glejaka wielopostaciowego
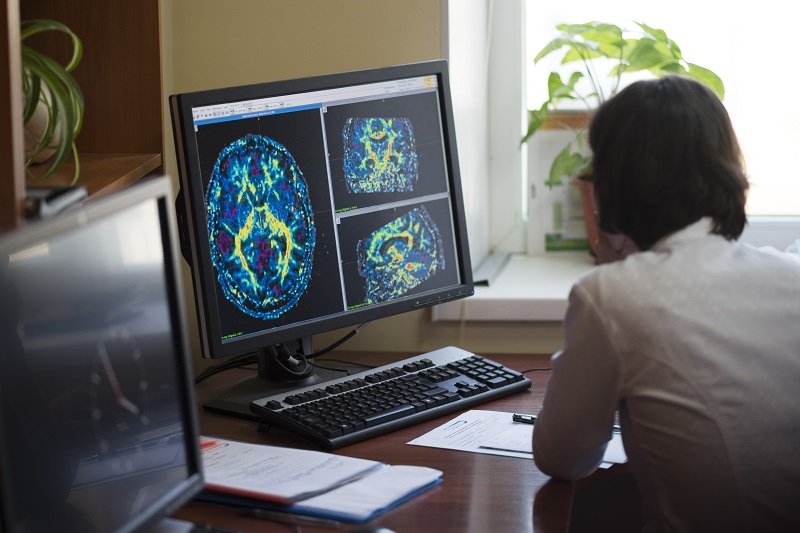
Glejak wielopostaciowy to najbardziej agresywny i złośliwy guz mózgu. Średni czas przeżycia chorego z rozpoznaniem glejaka wielopostaciowego, przy zastosowaniu obecnego standardu leczenia, to niewiele ponad 15 miesięcy. Mimo postępu jaki dokonał się w ostatnich latach w dziedzinie onkologii, wyniki leczenia złośliwych nowotworów mózgu pozostają niezadawalające.
Standardem w leczeniu złośliwych guzów mózgu pozostaje postępowanie chirurgiczne, czyli możliwe radykalna resekcja guza. Niestety, z uwagi na naciekający charakter wzrostu guza oraz położenie glejaka wielopostaciowego w obszarach mózgu, które uznaje się za nieoperacyjne, w wielu przypadkach przeprowadzenie radykalnego leczenia chirurgicznego bez uszkodzenia kluczowych obszarów mózgu nie jest możliwe.
– Za agresywnym charakterem wzrostu guza oraz jego opornością na nowe metody leczenia stoi m.in. unikalna zdolność komórek glejaka wielopostaciowego do hamowania odpowiedzi immunologicznej w organizmie człowieka. Główną rolę w rozpoznaniu komórki nowotworowej oraz jej zniszczeniu odgrywają limfocyty T. To one rozpoznają na powierzchni nowotworu specyficzne białka tzw. antygeny, a następnie generują immunologiczną, mającą na celu zwalczenie komórek nowotworu – wyjaśnia dr hab. n. med. Wojciech Kaspera.
I dodaje: – Z drugiej strony, komórki guza posiadają na swojej zewnętrznej powierzchni białka, nazywane fachowo tarczą molekularną, które zdolne są do blokowania tzw. punktów kontroli układu immunologicznego na powierzchni limfocytów T, co w efekcie prowadzi do ich inaktywacji i ucieczki nowotworu spod nadzoru układu immunologicznego. Innymi słowy, komórki nowotworowe wykorzystują tą tarczę by stać się niewidocznymi dla układu immunologicznego gospodarza.
PRZEJDŹ DO: RODZJAE GUZÓW MÓZGU
Projekt badawczy dotyczący glejaka wielopostaciowego wsparty przez Agencję Badań Medycznych zakłada wprowadzenie do terapii glejaka wielopostaciowego pembrolizumabu – leku blokującego receptor PD-1 (tzw. receptor programowalnej śmierci komórki), który obecny jest m.in. na powierzchni limfocytów T.
Nowotwór mózgu hamuje funkcję limfocytów T poprzez znajdujące się na jego powierzchni białko, które łącząc się z receptorem doprowadza do wygaszenia funkcji przeciwnowotworowej limfocytów T. Idea wykorzystania pembrolizumabu w terapii glejaka wielopostaciowego ma na celu przywrócenie aktywność limfocytów T i skuteczną walkę z nowotworem mózgu przy wykorzystaniu własnego układu immunologicznego.
– Przełomem w projekcie jest podejście, które zakłada włączenie pembolizumabu do leczenia przed planowanym leczeniem chirurgicznym. Zakładamy, że takie wykorzystanie inhibitora anty-PD-1 u pacjentów z rozpoznanym glejakiem wielopostaciowym może doprowadzić do aktywacji układu immunologicznego przed chirurgicznym usunięciem guza, a także wzmocni ono skuteczność stosowanych po leczeniu chirurgicznym metod uzupełniających leczenie takich jak chemioterapia i radioterapia – komentuje dr hab. n. med. Wojciech Kaspera.
Tego typu podejście to aktualnie jeden z najnowszych i najbardziej obiecujących trendów w badaniach klinicznych w obszarze onkologii. O dużej wartości innowacyjnej projektu świadczy założone w projekcie opracowanie nieinwazyjnej metody pozwalającej z jednej strony ocenić wskazania do zastosowania terapii pembrolizumabem, jak i monitorującej jego efektywność.
Do tego celu wykorzystane zostanie badanie immuno-PET (pozytonowa tomografii emisyjna) z wykorzystaniem innego inhibitora immunologicznych punktów kontroli odpowiedzi odpornościowej (atezolizumabu) znakowanego radioaktywnym cyrkonem. Będzie to pierwsze w Polsce wykorzystanie badania PET w immunoterapii.
źródła: www.abm.gov.pl, www.sum.edu.pl.
PRZEJDŹ DO: NAJNOWSZE WIADOMOŚCI