W maju 2020 roku Amerykańska Agencja Żywności i Leków (FDA) zarejestrowała na terenie Stanów Zjednoczonych olaparib w leczeniu pacjentów z przerzutowym, opornym na kastrację rakiem prostaty (ang. metastatic castration-resistant prostate cancer, mCRPC) z obecnością mutacji w genach naprawy DNA (m.in. BRCA1, BRCA2, ATM) u których doszło do progresji po terapii enzalutamidem lub abirateronem.
Decyzja FDA została oparta na wynikach badania klinicznego III fazy PROfound.
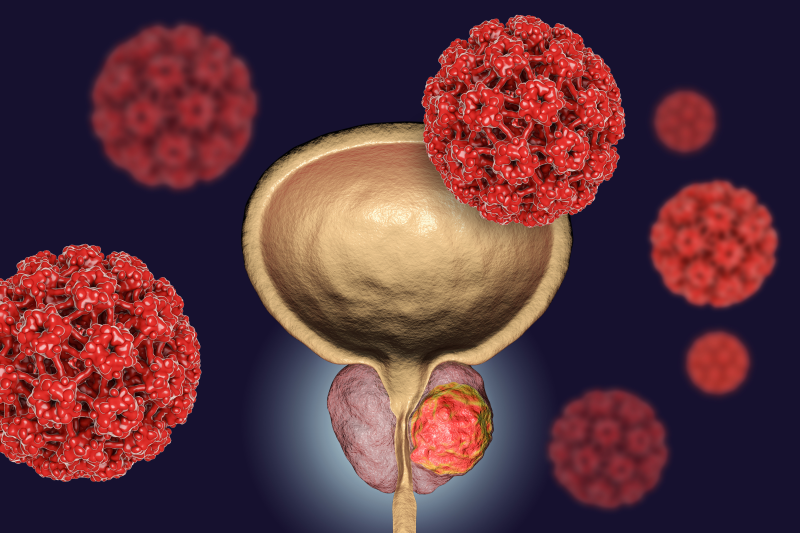
BRCA-dodatni rak prostaty
Skuteczność i bezpieczeństwo olaparibu w tym wskazaniu oceniano w otwartym, wieloośrodkowym badaniu klinicznym z randomizacją PROfound do którego włączono łącznie 387 chorych. Chorych przydzielono do ramienia otrzymujacego olaparib lub do ramienia otrzymującego leczenie zgodnie z wyborem badacza (enzalutamid lub octan abirateronu). U wszystkich chorych stosowano dodatkowo analogi gonadoliberyny lub poddano ich obustronnej orchidektomii.
Pacjentów z rakiem prostaty podzielono na dwie kohorty w zależności od statusu genów HRR: kohorta A (mutacje w genie BRCA1, BRCA2 lub ATM, n=245 chorych) lub kohorta B (mutacja w jednym z 12 genów HRR, n=142 chorych).
Okazało się, że najlepszą odpowiedź na leczenie olaparibem wykazali pacjenci z mutacją w genach BRCA. Dla kohorty A w ramieniu z olaparibem wykazano statystycznie istotne wydłużenie czasu wolnego od radiologicznej progresji choroby (rPFS), wydłużenie czasu przeżycia całkowitego (OS) oraz przewagę w zakresie odsetka obiektywnych odpowiedzi ORR.
BRCA-dodatni rak prostaty to kolejny nowotwór w którym wykazano potencjał terapeutyczny olaparibu. Inne nowotwory złośliwe to m.in. brca-zależny rak trzustki oraz rak jajnika).
Olaparib to inhibitor enzymów PARP biorących udział w naprawie DNA uszkodzonego podczas podziału komórki. Inhibitory PARP są szczególnie skuteczne w przypadku występowania mutacji w genach BRCA1 i/lub BRCA2.
źródło: www.fda.gov
ZOBACZ WIĘCEJ: NOWOTWORY BRCA-ZALEŻNE






















Mój maż z kolei miał to szczęście, że udało mu się w miarę „uciec” przed rakiem, dzięki operacji przy użyciu robota da vinci w szpitalu mazovia, naprawdę wszystko na spokojnie się udało i guza już nie ma. Ale teraz jak się wystraszył to się regularnie bada, cóż jak to mówią, mądry polak po szkodzie…