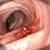
Nowotwory to druga z najczęstszych przyczyn zgonów w Polsce. W ostatnich latach zaobserwowano wzrost zachorowań na nowotwory złośliwe zarówno u polskich mężczyzn, jak i kobiet. Jak wskazują badania ekspertów – niektóre z groźnych nowotworów poprzedzane są wystąpieniem jednostek chorobowych, które predysponują do zwiększonego ryzyka zachorowania i nieleczone prowadzą do rozwoju raka. Jednym z takich zespołów jest rodzinna polipowatość gruczolakowata (FAP) – choroba dziedziczona w sposób autosomalny dominujący, predysponująca do zachorowania na raka jelita grubego.
Jej przyczyną są mutacje germinalne w genie APC (ang. adenomatous polyposis coli). O tym jakie są objawy rodzinnej polipowatości gruczolakowatej, na czym polega profilaktyka i leczenie zespołu FAP oraz jaki ma ona związek z rakiem jelit grubego opisuje dr n. med. Sylwia Łuczak, diagnosta laboratoryjny z Centrum Badań DNA w Poznaniu.
RODZINNA POLIPOWATOŚĆ GRUCZOLAKOWATA – INFORMACJE
Od pierwszego opisu rodzinnej polipowatości gruczolakowatej FAP w 1947 r., zespół ten został w znacznym stopniu zbadany i scharakteryzowany w literaturze. W 1975 roku Bussey przedstawił cechy kliniczne i historię naturalną FAP. Częstość występowania rodzinnej polipowatości gruczolakowatej to około 1/10000 żywo urodzonych i przejawia się jednakowo u obu płci, natomiast de novo choroba występuje z częstością 1 na 8000 – 10000 urodzeń. W Unii Europejskiej, częstość występowania szacuje się na 1 / 11,300-37,600.
Rodzinną polipowatość gruczolakowatą charakteryzuje rozwój w drugiej dekadzie życia, wielu dziesiątków do tysięcy gruczolaków, zlokalizowanych w odbytnicy i okrężnicy. Głównie są to polipy cewkowe o średnicy dochodzącej do kilku centymetrów, ale obserwuje się również polipy cewkowo-kosmkowe i kosmkowe. U połowy pacjentów z FAP polipy występują już około 15 roku życia, a w wieku 35 lat ma je już 95% chorych. Choroba zwykle nie ujawnia się przed 10. rokiem życia. Jej pełny obraz powstaje przeważnie w 3. – 4. dekadzie życia. Tylko wyjątkowo objawy rodzinnej polipowatości gruczolakowatej mogą się pojawić w okresie noworodkowym lub wczesnoniemowlęcym. Najmłodszym przypadkiem, u którego zaobserwowano polipy było 3-letnie dziecko. Polipy charakteryzują się dużym potencjałem rozwoju w kierunku nowotworu złośliwego, który może pojawić się począwszy od późnego dzieciństwa.
Wyodrębniono dwa główne fenotypy FAP, z uwagi na liczbę polipów oraz wieku, w którym wystąpiły pierwsze objawy:
- Klasyczny FAP – charakteryzuje się występowaniem setek do tysięcy polipów w okrężnicy i odbytnicy; do czasu osiągnięcia pełnoletniości, znajdowane polipy są raczej małe, dopiero z upływem czasu wzrasta ich liczba oraz wielkość. Nieleczony, prowadzi do rozwoju raka jelita grubego (ang. colorectal cancer, CRC), szybciej niż w przypadku przypadkowego CRC. Przeciętny wiek ujawnienia się nowotworu to 35 lat (rzadko poniżej 20 roku życia).
- AFAP (ang. attenuated FAP) – wariant FAP, z lżejszym przebiegiem, który charakteryzuje się późniejszym początkiem choroby, zmniejszoną liczbą polipów (10-100), przy czym często są one umiejscowione po prawej stronie jelita, a także zmniejszonym ryzykiem przekształcenia się w CRC.
Wyróżnia się również fenotyp związany z mutacjami w genie MUTYH (MAP), również ze skłonnością do występowania polipów jelita grubego, charakteryzujący się łagodniejszym przebiegiem, przy czym liczba polipów jest mniejsza niż w klasycznym FAP.
Jedną z postaci FAP jest również zespół Gardnera, w którym występowaniu setek czy tysięcy polipów w jelicie grubym towarzyszą kostniaki, guzy desmoidalne oraz przebarwienia siatkówki (CHRPE).
RODZINNA POLIPOWATOŚĆ GRUCZOLAKOWATA – OBJAWY I SYMPTOMY
Charakterystycznym objawem w zespole rodzinnej polipowatości gruczolakowatej są ogromne rzesze różnej wielkości polipów gruczolakowatych, zlokalizowanych głównie w ostatniej części okrężnicy oraz w odbytnicy. Mogą one współistnieć z polipowatością dna żołądka, polipami dwunastnicy oraz gruczolakami w jelicie cienkim. Jednakże większość pacjentów pozostaje asymptomatyczna przez wiele lat, aż gruczolaki stają się duże i liczne, przez co powodują krwawienia z odbytu, anemię a następnie przyczyniają się do rozwoju raka. Generalnie, nowotwór zaczyna się rozwijać dekadę po pojawieniu się polipów.
Choroba ta może również dawać niespecyficzne objawy, takie jak zaparcia lub biegunki, bóle brzucha, wyczuwalne powiększenie fragmentu brzucha i/lub utratę masy ciała. W przebiegu FAP można obserwować także pozajelitowe objawy, takie jak kostniaki, nieprawidłowości uzębienia (niewyrżnięte zęby, wrodzony brak jednego lub większej liczby zębów, nadliczbowe zęby, torbiele oraz zębiaki) czy wrodzony przerost nabłonka barwnikowego siatkówki (ang. congenital hypertrophy of the retinal pigment epithelium, CHRPE).
Zespołowi rodzinnej polipowatości gruczolakowatej mogą towarzyszyć również inne nowotwory złośliwe, takie jak:
- rak tarczycy – głównie rak brodawkowaty tarczycy (inne typy nowotworów złośliwych tarczycy są bardzo rzadkie) – tego typu nowotwór w zespole FAP może występować z częstością od 0,6% do 6,1%.
- gruczolakorak jelita cienkiego – mnogie gruczolaki występują u 50-90% chorych, a u 3-5% chorych może rozwinąć się gruczolakorak.
- hepatoblastoma – u dzieci z zespołem FAP występuje aż 750-7500 razy częściej niż w populacji ogólnej.
- rak trzustki – zespół powoduje 4,5-krotny wzrost ryzyka zachorowania na ten typ nowotworu.
- rak żołądka – mimo, że polipy w żołądku występują u połowy chorych, to ryzyko rozwinięcia się raka żołądka w krajach zachodnich jest bardzo niskie, znacznie wyższe występuje w krajach azjatyckich, gdzie ryzyko może być nawet 10-krotnie wyższe niż w populacji ogólnej.
- rak nadnerczy – gruczolaki nadnerczy występują 4 razy częściej niż w populacji ogólnej, jednak przebieg kliniczny nie odbiega od przypadków nie uwarunkowanych zespołem; rak nadnerczy w zespole FAP występuje rzadko.
- guzy mózgu – najczęstszym guzem OUN związany z FAP jest rdzeniak, stanowi około 80% guzów związanych z zespołem FAP, jednakże ryzyko zachorowania w ciągu życia wynosi około 1%; występowanie tego rodzaju nowotworów w połączeniu z objawami FAP określa się mianem zespołu Turcota.
GENETYKA W ZESPOLE FAP
Po raz pierwszy, jako przyczynę FAP, opisano w 1991 r. mutacje germinalne w genie adenomatous polyposis coli (APC), z autosomalnie dominującym wzorem dziedziczenia. Gen APC zlokalizowany jest na chromosomie 5q21-22 i bierze udział w kontroli proliferacji komórek. Część kodująca genu składa się z 15 eksonów i koduje białko zbudowane z 2843 aminokwasów. Ponadto, pierwsze eksony genu mogą tworzyć tkankowo specyficzne alternatywne transkrypty. Charakterystyczną cechą tego genu jest występowanie dużego eksonu 15, który obejmuje ponad 70% sekwencji kodującej. Większość mutacji germinalnych w genie APC skutkuje skróconym produktem białkowym.
Obecnie zidentyfikowano ponad 1000 mutacji, przy czym najliczniejszą grupę stanowią małe delecje (ponad 350). Drugie w kolejności są substytucje jednonukleotydowe prowadzące do zamiany aminokwasu lub powstania kodonu terminacyjnego. Opisano również duże delecje, mutacje splicingowe, indel, duże insercje, rearanżacje kompleksowe oraz mutacje w miejscach regulatorowych. Ponadto około 25% pacjentów z FAP jest nosicielami mutacji de novo.
W 2002 r., zidentyfikowano kolejny gen związany z polipowatością – mutY homolog (MUTYH). Mutacje w tym genie tworzą autosomalnie recesywny wzór dziedziczenia. Zmiany w obrębie tego genu prowadzą do MAP (ang. MUTYH–associated polyposis). Forma recesywna FAP związana jest z homozygotycznymi mutacjami w genie MUTYH. Gen MUTYH, zlokalizowany w locus 1p34.3-32.1, zaangażowany jest w naprawę oksydacyjnych uszkodzeń DNA. Składa się z 16 eksonów i koduje białko zbudowane z 535 aminokwasów. Charakterystycznym jest to, że żaden z 15 intronów nie jest większy niż 200 bp. Do tej pory zidentyfikowano ponad 80 patogennych mutacji, z czego najliczniejsze są missensowne substytucje a następnie mutacje typu „splice site”. Znaleziono również nieliczne duże delecje, mutacje zmiany ramki odczytu oraz mutacje nonsensowne. Zmiany dotknęły praktycznie wszystkie eksony, z wyjątkiem 1 i 2. Zidentyfikowano również dwie mutacje „hot spot”, które występują w 70-80% przypadkach o europejskim pochodzeniu. Są to mutacje p.Y179C (c.536A>G) oraz p.G396D (c.1187G>A).
ZESPÓŁ RODZINNEJ POLIPOWATOŚCI GRUCZOLAKOWATEJ – DIAGNOSTYKA I LECZENIE
Większość pacjentów (~70%) ma w wywiadzie rodzinnym przypadki polipów czy raka jelita grubego. Diagnostyka opiera się na zebraniu wywiadu rodzinnego, analizie objawów klinicznych i endoskopii lub pełnej kolonoskopii jelita grubego. Jeśli to możliwe, rozpoznanie kliniczne powinno być potwierdzone również badaniami genetycznymi.
W pierwszym etapie rozwoju dochodzi do sporadycznych krwawień z odbytu i biegunek a w dalszej kolejności do spadku masy ciała czy anemii. To powinno być pierwszą przesłanką do podejrzenia FAP oraz zlecenia wykonania endoskopii jelita. Gdy lekarz stwierdzi obecność powyżej 100 polipów, należy przyjąć, iż przyczyną w/w objawów jest właśnie rodzinna polipowatość gruczolakowata. Wiek występowania objawów u chorych jest dość zróżnicowany, obserwuje się również różnice w wieku występowania objawów u rodzeństwa. Jednak można przyjąć, że wystąpienie raka jelita grubego w młodym wieku powinno być sygnałem do przeprowadzenia wywiadu rodzinnego, który pozwala na określenie, czy w rodzinie występuje wysoka dziedziczna predyspozycja. Występowanie pojedynczego przypadku choroby nie wyklucza wysokiej dziedzicznej predyspozycji, ponieważ chory może być pierwszym nosicielem mutacji.
W przypadku pojawienia się polipów jedynym wyjściem jest operacyjne usunięcie całego jelita grubego. Pozwoli to, w dużym stopniu, uniknąć wystąpienia nowotworu inwazyjnego. Profilaktyczna kolektomia wykonana w odpowiednim czasie i w odpowiedni sposób pozwala na wydłużenie życia chorych z FAP średnio z 45 do 60 lat. Podjęto również próby leczenia profilaktycznego w postaci podawania niesteroidowych leków przeciwzapalnych, np. celekoksybu, sulindaku. Profilaktyka w kontekście zespołu rodzinnej polipowatości gruczolakowatej to obecnie głównie sigmoskopia lub kolonoskopia wykonywana co 12 miesięcy, począwszy od 10-11 roku życia. Raz do roku powinno się również wykonywać ezofagogastroduodenoskopię (gastroskopia całego górnego odcinka przewodu pokarmowego) u osób od 25 roku życia lub w przypadku pojawienia się polipów. Zalecane jest również badanie USG tarczycy.
Podsumowując, nierozpoznanie FAP i nie poddanie się leczeniu, prowadzi praktycznie w 100% do rozwoju raka jelita grubego. W kontekście profilaktyki raka (a w szczególności u osób pochodzących z rodzin, w których często występują nowotwory) warto rozważyć przeprowadzenie specjalistycznych badań genetycznych DNA, np. panelu nowotworowego „ABC Nowotworów”, w celu wykrycia u danej osoby zwiększonego ryzyka rozwoju choroby nowotworowej.
Rodzinna polipowatość gruczolakowata, opracowała dr n. med. Sylwia Łuczak, diagnosta laboratoryjny, Centrum Badań DNA, Poznań,
źródła:M.L. Leoz i wsp. „The genetics basis of familial adenomatous polyposis and its implications for clinical practice and risk management”, The Application of Clinicial Genetics 2015:8 95-107; Plawski i wsp. “Familial adenomatous polyposis of the colon”, Hereditary Cancer in Clinical Practice 2013 11:15; M.H. Nieuwenhuis, H.F.A. Vasen “Correlations between mutation site in APC and phenotype of familial adenomatous polyposis (FAP): A review of the literature”, Critical Reviews in Oncology/Hematology 2007(61): 153-161
ZOBACZ: STRONA GŁÓWNA